단일기관 응급실에서 시행한 90일 미만 발열 환자에 대한 Step-by-Step approach의 후향적 타당도평가
Retrospective validation of the Step-by-Step approach for febrile infants younger than 90 days in the emergency department
Article information
Trans Abstract
Purpose
To retrospectively validate the Step-by-Step approach, a sequential algorithm for prediction of serious bacterial infections (SBI) using the appearance, age, and inflammatory markers, in febrile infants younger than 90 days.
Methods
The presence of SBI was reviewed in febrile infants younger than 90 days undergoing blood and urine cultures (using perineal adhesive bags), assays for procalcitonin, C-reactive protein and absolute neutrophil count, and urinalysis at the emergency department from September 2015 through August 2017. The low-risk infants were classified according to the Step-by-Step approach. SBI was defined as urinary tract infection (UTI), bacteremia or meningitis. We measured the sensitivity and negative predictive value (NPV) of the approach in predicting SBI, and compared the values to those of the Rochester criteria and the Lab-score.
Results
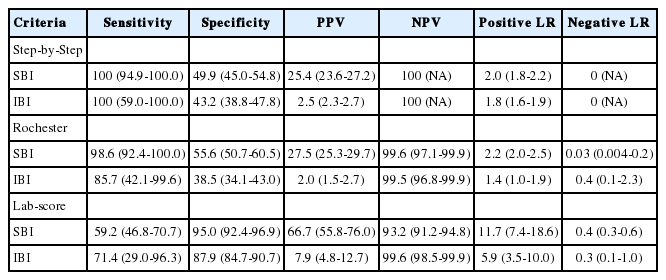
Of 488 febrile infants (44.7% underwent lumbar puncture), 71 (14.5%) had SBI, including 67 UTI, 5 bacteremia, and 3 meningitis (mutually inclusive). Of 208 low-risk infants (42.6%), no SBI was found. The Step-by-Step approach showed a 100% sensitivity (95% confidence interval [CI]: 94.9-100.0) and NPV (95% CI: not applicable). The Rochester criteria showed a 98.6% sensitivity (95% CI: 92.4-100.0) and 99.6% NPV (95% CI: 97.1-99.9), and missed 1 meningitis. The Lab-score showed a 59.2% sensitivity (95% CI: 46.8-70.7) and 93.2% NPV (95% CI: 91.2-94.8), and missed 2 meningitis and 27 UTI.
Conclusion
The Step-by-Step approach showed a 100% sensitivity and NPV in predicting SBI. This approach may help predict SBI without lumbar puncture in febrile infants younger than 90 days.
서론
90일 미만 발열 환자에서 serious bacterial infection (SBI)의 저위험군을 선별하기 위해, 필라델피아 기준[1]이 자주 사용된다. 13가 폐렴구균백신 보급 이후, 90일 미만 발열 환자의 세균혈증과 수막염의 빈도는 각각 2.6%와 0.3%이며[2], 그 원인균 중 Streptococcus pneumoniae의 비율은 감소했다[3,4]. 2011-2013년에 미국의 32개 병원을 방문한 29-56일 발열 환자 대상 연구는 일상적 요추천자가 예후와 연관이 없음을 제시했다[5]. 또한, 같은 나이의 환자 1,188명에게 요추천자를 시행한 결과, 수막염 환자는 필라델피아 고위험군 1명이었다[6].
2013년에 발표된 “Step-by-Step approach” (Fig. 1)는 요추천자 없이 외양과 나이, 염증표지자 4종(혈액 프로칼시토닌, C-반응단백질, 적대호중구수, 소변 백혈구)을 단계적으로 검토하는 저위험군 기준이다[7]. 한 전향적 타당도평가에서 이 기준의 민감도와 음성예측도를 각각 92.0%와 99.3%로 보고했고, 이는 로체스터 기준[8]보다 우수했다[9]. 한국에서는 2014년에 13가 폐렴구균백신이 국가예방접종에 포함됐으므로, 유사한 민감도와 음성예측도가 나올 것으로 기대된다. 본 연구는 단일기관 응급실을 방문한 90일 미만 발열 환자에서 Step-by-Step approach의 SBI예측 타당도를 평가하기 위해 시행했다.
대상과 방법
1. 연구대상
본 후향적 연구는, 2015년 9월부터 2017년 8월까지 단일 삼차의료기관 응급실(소아환자 연간 약 35,000명 방문)을 방문한 90일 미만 발열(고막 체온 ≥ 38℃) 환자 중, 혈액 및 소변 배양, 프로칼시토닌, C-반응단백질, 절대호중구수, 요검사를 모두 시행한 환자를 대상으로 시행했다. 상기 검사 미시행, 외부병원 이송, 예방접종 후 발열, 임상적 바이러스감염에 해당하는 환자는 제외했다.
아파 보이는 환자는 검사결과와 무관하게 요추천자, 항생제 치료 및 입원을 시행하고, 그렇지 않은 환자는 C-반응단백질 > 2 mg/dL, 프로칼시토닌 ≥ 0.5 ng/mL 또는 농뇨가 있으면, 상기 검사 및 처치를 시행했다. 입원 환자 중, 세균혈증 또는 수막염 환자는 2-3주간 항생제 치료를 지속하며 배양 음전을 확인했다. 요로감염 환자는 항생제 치료 후 체온이 정상화되면 퇴원했고, 이후 외래에서 배양 음전을 확인했다. 초기 배양 음성 환자는 체온과 C-반응단백질 농도가 정상화되면 퇴원했다. 본 연구는 서울아산병원 임상연구심의위원회의 승인을 받고 시행했다(IRB No. 2017-0918).
2. 자료수집
나이(< 90일), 체온(≥ 38℃), 검사코드(프로칼시토닌, C-반응단백질, 백혈구계산)로 환자를 검색했다. 통계적 분석 과정에서 각 연구대상자의 독립성을 추구하기 위해, 2회 이상 방문은 첫 번째 방문만 포함했다. 임상변수로, 나이(일), 성별, 발열 지속시간(시간), 아파 보이는 외양 유무, 체온, 호흡기 증상, 소화기 증상, 피부병소를 수집했다. 외양 평가는 담당의에 따라 다양한 방법으로 시행했다. 이 때문에, 의무기록에 ‘아파 보임’, ‘전신상태 불량’, ‘처짐’, ‘탈수’, ‘호흡곤란’, ‘보챔’, ‘청색증’, ‘창백’, ‘얼룩덜룩한 피부’ 중 한 가지 이상이 기록되면, 아파 보이는 외양으로 간주했다[7,10]. 실험실검사 변수로는 배양 결과(혈액, 소변, 뇌척수액)를 수집하고, 그 외에는 혈액에서 프로칼시토닌, C-반응단백질, 절대호중구수, 백혈구계산 결과를, 요검사에서 농뇨(≥ 10/high-power field, 백혈구에스테라아제 또는 아질산염 양성) 여부를 기록했다. 예후 변수로는 발열로 1주 이내 본원 재방문 후 입원, 입원 기간(일), 중환자실 입원, 원내사망 여부를 수집했다. 귀가 후 발생한 추가 진단 및 합병증 유무를 조사하지 못했다.
3. 용어 정의
1) SBI
혈액, 소변 또는 뇌척수액 배양에서 세균이 확인된 경우로 정의했다. 영아 요로감염 진단은 도뇨관을 이용한 요배양에 기초해야 한다[11]. 다만, 본 연구에서는 무균채뇨백뇨를 사용했으므로, 농뇨와 함께 단일 세균이 105 colony-forming unit/mL 이상 확인되면 요로감염으로 간주했다. 농뇨 없이 상기 요배양 결과가 확인되면, 잠재요로감염(possible urinary tract infection)으로 정의했다.
2) Invasive bacterial infection (IBI)
혈액 또는 뇌척수액 배양에서 세균이 확인된 경우로 정의했다. 이는, SBI 중 요로감염의 비율과 세균혈증 원인균 중 Escherichia coli의 비율이 증가하는 추세[3]에서 요추천자 필요성이 큰 환자의 빈도를 분석하기 위한 것이다.
3) 오염
배양에서 coagulase-negative staphylococci, viridans group streptococci (감염심내막염 제외), Micrococcus spp., Corynebacterium spp., Neisseria meningitidis 또는 N. gonorrhoeae 외 Neisseria spp.가 확인되면 오염으로 정의했다. 또한, 의무기록에 오염으로 기재됐거나 배양 양성에도 불구하고 항생제를 투여하지 않으면, 오염으로 간주했다.
4. Step-by-Step approach 후향적 타당도평가
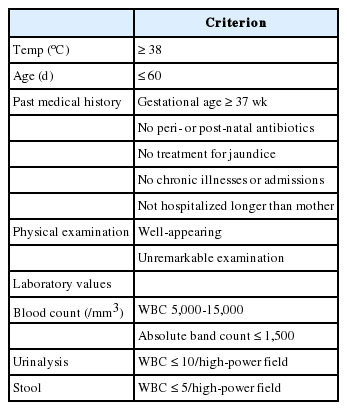
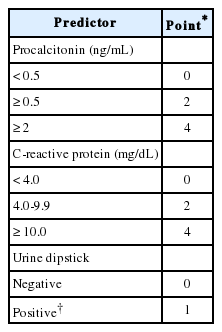
연구대상자에게 Step-by-Step approach를 적용했다. 아파 보이는 외양, 생후 21일 이하, 농뇨, 프로칼시토닌 ≥ 0.5 ng/mL, C-반응단백질 > 2 mg/dL 또는 절대호중구수 > 10,000/mm3 순으로 적용하여, 이 기준에 모두 해당하지 않으면 저위험군으로 정의했다(Fig. 1). 저위험군에서 SBI, 잠재요로감염 빈도를 측정했다. Step-by-Step approach의 예측 타당도를 요추천자를 포함하지 않는 다른 저위험군 기준과 비교하기 위해, 별도로 로체스터 기준[8](Appendix 1)과 Lab-score [12] (Appendix 2)에 따라 저위험군을 분류했다. 단, 로체스터 기준에 필요한 절대띠호중구수는 검사 빈도가 낮아 분석에서 제외했다.
5. 통계적 분석
연속형 변수는 정규분포 여부에 따라 평균 및 표준편차 또는 중앙값 및 사분위수 범위로, 범주형 변수에 대해서는 환자 수와 비율로 각각 기술했다. 세 기준에 따른 저위험군 환자에서 SBI 및 IBI에 대한 민감도, 특이도, 양성 및 음성예측도, 양성 및 음성 우도비, 각 변수의 95% 신뢰구간을 계산했다. 저위험군 기준임을 고려하여, 세 기준의 민감도와 음성예측도를 비교했다. 이 과정에 MedCalc Statistical Software ver. 17.8.6 (MedCalc Software bvba, Ostend, Belgium)을 사용했다.
결과
1. 일반적 특성
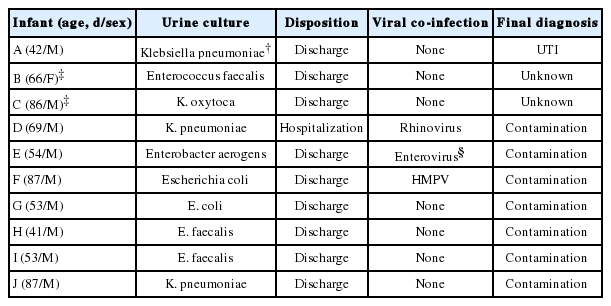
연구기간에 응급실을 방문한 90일 미만 발열 환자 670명 중, 혈액 및 소변 배양, 프로칼시토닌, C-반응단백질, 절대호중구수, 요검사를 모두 시행한 488명(72.8%)을 등록했다(Fig. 2). 제외 환자 중, SBI는 18명(9.9%; 95% 신뢰구간, 6.0-15.2), IBI는 group B streptococcus 수막염 1명(0.5%; 95% 신뢰구간, 0.01-3.0)이었다. 연구대상자 나이의 중앙값은 59.0일(사분위수 범위, 39.0-73.0일)이었고, 남자가 274명(56.1%), 21일 이하는 49명(10.0%; 28일 미만, 70명[14.3%])이었다. 아파 보이는 환자는 93명(19.1%)이었고, 요추천자는 218명(44.7%)에게 시행했다. SBI 환자는 71명(14.5%; 95% 신뢰구간, 11.5-18.0)으로 이 중 요로감염이 가장 흔했고, IBI는 7명(1.4%; 95% 신뢰구간, 0.6-2.9)이었다(Table 1).
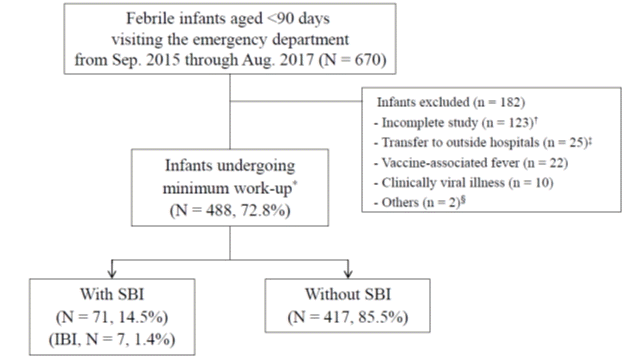
Flowchart for the selection of infants. *Blood and urine cultures (using perineal adhesive bags), assays for procalcitonin, C-reactive protein, and absolute neutrophil count, and urinalysis. †Mostly, procalcitonin was omitted. ‡Without work-up due to the limited capacity of the study setting. §One infant was sent directly to the intensive care unit, and the other’s guardians refused work-up. SBI, serious bacterial infection; IBI, invasive bacterial infection.
진료결과는 귀가 239명(49.0%), 입원 232명(47.5%; 중환자실 4명), 전원 17명(3.5%)이었다. 1주 이내 본원 재방문 환자 24명 중, 10명이 입원했다. 이 중 1명이 요로감염이었지만, 초기 배양 음성이었으므로 SBI가 아닌 것으로 간주했다. 중환자실 입원 4명은 모두 Step-by-Step 및 로체스터 고위험군이었지만, 이 중 SBI 환자는 없었다. 이 중 원내 사망은 초기 배양 음성을 보인 80일 남자 1명이었는데, 입원 후 흉수 배양에서 Klebsiella pneumoniae, Enterobacter spp.가 확인됐고 폐렴에 의한 급성호흡곤란증후군으로 사망했다. 그 외 3명 중 2명은 각각 호흡기세포융합바이러스 폐렴과 Staphylococcus epidermidis 세균혈증(초기 배양 음성)이었고, 1명은 원인 미상이었다.
2. 세 저위험군 기준의 민감도와 음성예측도 비교
Step-by-Step approach의 민감도와 음성예측도는 모두 100%로, 로체스터 기준과 통계적 차이가 없었고 Lab-score보다 우수했다(Table 2). Step-by-Step 저위험군 환자는 208명(42.6%)이었고 이 중 SBI 환자는 없었다. 로체스터 저위험군(186명, 38.1%)에 수막염 환자 1명(S. bovis), Lab-score 저위험군(425명, 87.1%)에 수막염 환자 2명(E. coli, S. bovis)과 요로감염 환자 27명이 각각 포함됐다(Table 3).
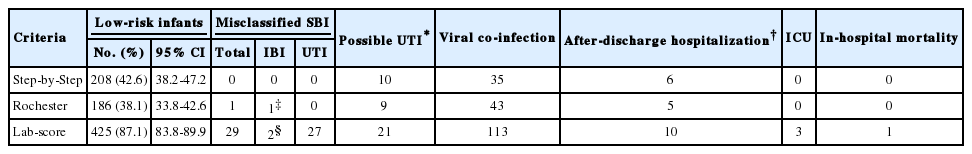
Misclassified serious bacterial infection among low-risk infants according to the 3 low-risk criteria
Step-by-Step 저위험군에서 잠재요로감염 환자는 10명으로, 이 중 3명은 바이러스감염에 동반한 오염으로 확인됐다(Appendix 1). 나머지 7명 중 5명이 외래를 방문했고, 이 중 1명이 요로감염으로 확인됐다. 이 1명에 외래를 방문하지 않아 최종진단을 알 수 없는 2명을 합한 총 3명을 요로감염으로 간주하면, Step-by-Step approach의 SBI에 대한 민감도는 95.9% (95% 신뢰구간, 88.6-99.2), 음성예측도는 98.6% (95% 신뢰구간, 95.7-99.5)였다.
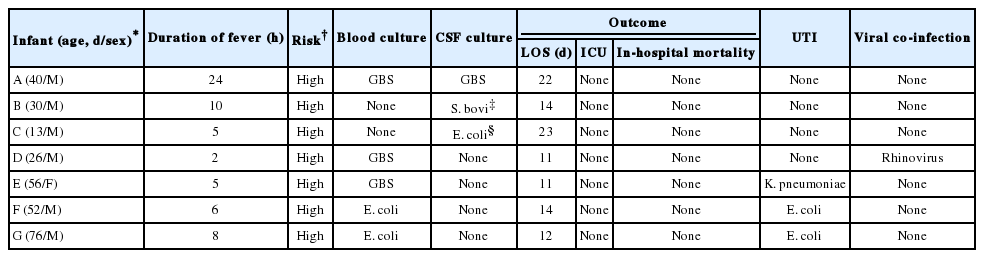
3. SBI 환자의 미생물 진단과 예후
세균혈증 환자 중 2명은 E. coli에 의한 요로성패혈증이었고, group B streptococcus 세균혈증 환자 3명 중 2명은 각각 같은 세균에 의한 수막염과 K. pneumoniae 요로감염을 동반했다(Table 4). IBI 환자 7명 모두 프로칼시토닌 ≥ 0.5 ng/mL였다. 그 외 Step-by-Step approach 구성요소에 해당하는 환자 수는 아파 보이는 외양과 C-반응단백질 ≥ 2 mg/dL 각 4명, 농뇨 3명, 절대호중구수 > 10,000/mm3 2명, 생후 21일 이하 1명이었다. 요로감염 원인균으로 E. coli가 가장 흔했고(56명), 이어서 K. pneumoniae (6명), Enterobacter spp. (3명), Enterococcus spp. 및 group B streptococcus (각 1명) 순이었다. SBI 환자 71명 중, 중환자실 입원 및 원내사망은 발생하지 않았다. 바이러스 동시감염을 보인 12명 중, 1명만 호흡기 증상을 보였다.
고찰
본 연구의 임상적 의의는 두 가지로 요약할 수 있다. 첫째, 요추천자가 필요한 필라델피아 기준 대신 Step-by-Step approach로써, 90일 미만 저위험군 발열 환자를 선별할 수 있음을 시사한다. 둘째, 상기 환자군의 약 40%를 차지하는 저위험군에서 잠재적으로 불필요한 요추천자를 줄일 수 있음을 시사한다. 불필요한 요추천자는 외상천자, 뇌탈출, 경막외출혈, 요통 및 두통, 환자 및 보호자의 불편을 초래할 수 있다[13,14]. 2003-2013년에 스페인에서 시행된 연구에서 90일 미만 발열 환자 2,362명 중 수막염 환자는 11명(0.5%)이었고, 모두 21일 이하이거나 아파 보였다[15]. 따라서, 저위험군에서는 요추천자를 신중하게 시행해야 한다.
단일기관 후향적 연구임에도 본 연구결과를 비교적 신뢰할 수 있는 이유는 다음과 같다. Step-by-Step approach 구성요소 중 정확도가 낮다고 알려진 외양[16]을 제외한 나이, 혈액 및 소변 염증표지자는 객관적으로 기록했다. 나이, 성별, 아파 보이는 외양과 입원 빈도는 2016년에 발표된 같은 기준의 전향적 타당도평가 결과와 유사했다[9]. 요추천자 빈도는 미국의 37개 어린이병원에서 보고한 빈도(41.4%)와 유사했다[17]. 세균혈증과 수막염 빈도가 미국의 대규모 연구결과와 유사한 점은[2], 선택치우침의 영향이 크지 않았음을 시사한다.
Step-by-Step approach 및 로체스터 기준의 민감도와 음성예측도는 Lab-score보다 우수했다. 이는 일차적으로 요로감염 예측과 관련이 있다. 요로감염 진단에 농뇨가 필요하고[18] 농뇨가 있으면, Step-by-Step 및 로체스터 고위험군으로 분류된다. Mintegi 등[7]의 보고에 의하면, Step-by-Step 저위험군에 요로감염 환자 없이 세균혈증 환자 1명만 포함됐다. 반면, Lab-score 고위험군은 3점 이상으로 정의하며, 농뇨에 1점을 부여한다[12]. 즉 낮은 프로칼시토닌 또는 C-반응단백질 농도를 보이는 요로감염 환자는 저위험군으로 분류될 수 있다. 이는 본 연구에서 Lab-score 저위험군에 요로감염 환자 27명이 포함된 것으로 뒷받침할 수 있다. Lab-score 구성요소에 외양과 나이가 없는 점[12]도 낮은 민감도와 음성예측도에 기여했을 것이다.
본 연구에서 Step-by-Step 및 로체스터 저위험군 간의 중요한 차이는 후자에 수막염 환자가 1명 포함된 점이다. 이는 Step-by-Step 및 로체스터 저위험군 환자 중 IBI 빈도가 각각 0.2%-0.7%와 1.1%-1.6%로 보고된 것과 일맥상통한다[7,9]. 이 차이는 전자에 프로칼시토닌이 포함된 것에 기인한 것으로 생각한다. 프로칼시토닌은 내독소 주입 4시간 이내에 측정 가능한 혈중농도로 상승하므로, 초기 SBI 예측에 유리하다[19,20]. 로체스터 저위험군의 수막염 환자는 발열 시작 10시간 후 아파 보이지 않는 상태로 방문했고, 백혈구계산은 정상 범위, 프로칼시토닌 농도는 1.4 ng/mL였다. 모든 IBI 환자의 프로칼시토닌 농도가 고위험군에 해당한 점은, Step-by-Step approach가 아파 보이지 않는 외양과 정상 백혈구계산 결과를 가진 환자의 세균혈증 및 수막염 예측에 있어서 로체스터 기준보다 우수함을 시사한다.
본 연구는 단일기관 후향적 연구에 내재한 제한점 외에도 몇 가지 제한점을 지닌다. 첫째, 적은 IBI 환자 수, 발열 환자의 72.8%만 혈액 및 소변 배양을 시행한 점, 귀가 후 추적조사의 결여가 Step-by-Step approach 음성예측도의 과대평가를 초래했을 수 있다. 그러나, 연구대상 및 제외 환자의 SBI 및 IBI 빈도에 통계적 차이가 없었으므로, 그 개연성은 작다고 본다. 둘째, 무균채뇨백 이용이 요로감염 빈도를 과대평가하는 데에 기여했을 수 있다. 이 점은 도뇨관을 이용한 연구로 보완할 수 있을 것이다. 셋째, Step-by-Step approach의 다른 구성요소와 달리, 외양 평가가 체계적이지 못했다. 하지만, Gomez 등9)이 보고한 아파 보이는 외양 빈도(12.3%)와 저위험군 비율(45.3%)이 본 연구의 수치와 유사하므로, 그 영향은 적었을 것으로 추정한다.
본 연구에서 Step-by-Step approach를 통해 90일 미만 발열 환자 중 42.6%를 저위험군으로 분류했고, SBI에 대한 민감도와 음성예측도는 100%였다. 이 환자군에 Step-by-Step approach를 적용한다면, 잠재적으로 불필요한 요추천자를 다소 줄일 수 있을 것으로 기대한다.
Notes
이해관계
본 저자는 이 논문과 관련된 이해관계가 없음.
Acknowledgements
본 저자는 이 논문과 관련된 재정지원을 받지 않았음.